Colesterol, Hipercolesterolemia
y Medicina Racional
Para todos los que deseen entender cómo el colesterol afecta la salud cardiovascular, y cómo funcionan las medicinas que reducen el colesterol. Lo he escrito en un tono informal y a un nivel que pueda entender cualquier estudiante de biología de escuela superior.
Éste es el primer draft, necesito arreglar la prosa y algunas de las ilustraciones. :-)
¿QUE ES EL
COLESTEROL, Y PARA QUE SIRVE?
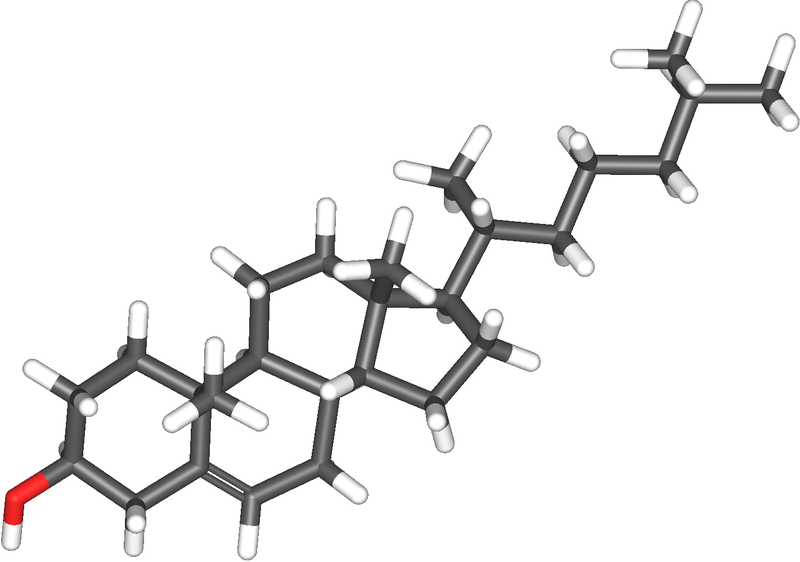
El colesterol es una molécula de la familia de los
lípidos. Es un esterol, que significa una combinación de esteroide con alcohol.
Tiene roles muy importante en el organismo, tales
como:
· > Rol estructural crítico en la
composición de las membranas de las células
o
aproximadamente la mitad de la bicapa
lípida que compone las membranas celulares está compuesta de colesterol
o
aproximadamente la mitad del
colesterol en el cuerpo humano está en las membranas celulares
o
el colesterol le da rigidez a las
membranas
· > Rol crítico en la producción de
varias sustancias, el colesterol es la molécula precursora de:
o
las hormonas esteroides (por ejemplo,
el estrógeno) y los glucocorticoides.
o
la vitamina D
o
los ácidos bílicos producidos por el
hígado y enviados a los intestinos para ayudar a emulsificar las grasas
¿DE DÓNDE
SALE EL COLESTEROL?
El colesterol en nuestro cuerpo proviene de dos
fuentes principales:
nuestra
dieta : huevos, carnes, etc.
biosíntesis: si no consumimos suficiente colesterol, nuestro cuerpo fabrica el que necesita. Esto se logra mediante una ruta metabólica bioquímica (biochemical pathway) bastante larga y compleja.
Esta es la versión abreviada:
ácido acético (CH3 COOH) → acetil-CoA → (...etc...)
→ HMG-CoA → Mevolonate → (...etc...) →
colesterol ↑
HMG-CoA
reductase
La reacción de conversión de HMG-CoA a mevolonate es
mediada por una enzima, HMG-CoA reductase. Una vez que ocurre ese paso, la
conversión a colesterol está determinada.
La ruta completa está disponible aquí:
¿CÓMO SE
TRANSPORTA EL COLESTEROL?
El colesterol es una molécula muy hidrofóbica. Por lo
tanto para poderlo transportar mediante el torrente sanguíneo hacia las células
que lo necesitan, es necesario “empacarlo” en partículas. Existen varios tipos
de partículas con diferentes formas y densidades:
1.
VLDL : Lipoproteína de muy baja densidad
2.
LDL : Lipoproteína de baja densidad
3.
IDL : Lipoproteína de densidad intermedia
4.
HDL : Lipoproteína de alta densidad
5.
quilomicrones: moléculas de baja densidad y gran
tamaño
Éstas partículas son sintetizadas en el hígado
mediante la siguiente ruta:
VLDL
→
IDL → LDL : ésto ocurre en el torrente sanguíneo
↕
HDL : en éste punto se intercambian HDL por
moléculas de triglicéridos
¿CUAL ES LA
RELACIÓN ENTRE LÍPIDOS Y ENFERMEDADES CARDIOVASCULARES?
·
1850s:
o
La hipótesis de los lípidos proponía
que la concentración de lípidos en la sangre correlaciona con los ataques
cardíacos.
o
evidencia de autopsias: placas de
grasa y lípidos presentes en los corazones de cadáveres que morían de ataques
al corazón
o
evidencia experimental: se
alimentaron conejos con una dieta alta en grasas, y desarrollaron síntomas
similares a los de aterosclerosis.
§
PERO los conejos no son un modelo
exacto de los seres humanos
·
1950s:
o
estudios epidemiológicos en seres
humanos determinaron que las personas con altos niveles de colesterol tenían
una probabilidad mayor de sufrir ataques al corazón
o
NO es altos niveles de colesterol en
general sino de UNA forma de colesterol en particular : LDL
·
Hoy:
o
se ha podido ir más allá de una mera
correlación y se ha demostrado una relación causal
o
Las placa ateroscleróticas están
compuestas de proteínas, lípidos y colesterol
o
Éstas placas obstruyen los vasos
sanguíneos, hacen que las paredes de los vasos sanguíneos se endurezcan.
o
Pedacitos pequeños de las placas se
desprenden y pueden obstruir completamente los vasos sanguíneos pequeños.
o
Ese bloqueo impide que llegue sangre
con oxígeno a las células que dependen de esos pequeños vasos sanguíneos, lo
que causa su muerte.
o
Ésto es lo que se conoce como un
infarto.
o
altos niveles de HDL = riesgo de
ataque al corazón se reduce
o
altos niveles de LDL = riesgo de
ataque al corazón aumenta
¿CUAL ES EL
ROL DEL HÍGADO?
Una de las funciones del hígado es recoger el exceso
de LDL de la sangre y usarlo para sintetizar otros compuestos, como por ejemplo
ácido bílico. Para que ésto ocurra, las células del hígado tienen una proteína
receptora en su superficie conocida como LDL-R, el receptor de LDL. Las
moléculas de LDL se enlazan con éste receptor, y ésto le da una señal a la
célula para que absorba ese LDL y lo use.
Sin embargo, en algunas personas el gen que produce
esa proteína receptora tiene al menos un alelo cuya mutación resulta en la
ausencia del receptor LDL-R. Las personas con ésta mutación tienen una capacidad
reducida de eliminar el LDL de su sangre.
Cuando una célula hepática (hígado) tiene una cantidad
baja de colesterol, va a aumentar la expresión (upregulate) del gen que produce HMG CoA reductase (para sintetizar
colesterol por sí misma) o va a aumentar la expresión del gen que produce LDL-R
(para capturar colesterol de la sangre). De la misma manera, cuando una célula
tiene una cantidad excesiva de colesterol, va a reducir la expresión (downregulate) de los genes que producen
LDL-R y HMG CoA reductase.
¿CUÁLES SON
LOS ASPECTOS GENÉTICOS DE LA HIPERCOLESTEROLEMIA?
La mutación genética que causa el alelo FH tiene como
consecuencia alteraciones en los procesos de síntesis, degradación y remoción
del LDL de la sangre. Por lo tanto, las personas con el alelo recesivo FH
tienen mayores niveles de LDL y mayores probabilidad de desarrollar
enfermedades cardiovasculares. Ésta mutación se comporta como una característica mendeliana recesiva simple:
Normal ( + / +)
|
Heterocigoto (FH / +)
|
Homocigoto (FH/FH)
|
|
LDL
|
100
mg/dL
|
250
mg/dL
|
>
600 mg/dL
depósitos
visibles
|
riesgo de ataque al corazón
|
normal
|
10
– 20 años antes de lo normal
prevalencia:
1 de cada 500 personas es heterozigoto
|
antes
de los 20 años
prevalencia:
1 en 1 millón de personas es homozigoto al alelo recesivo.
|
(+/+) : personas que
tienen el alelo normal del gen en ambas copias
(FH/+): personas que tienen
el alelo normal en una copia y el mutante FH en otra
(FH/FH): personas que tienen el alelo mutante
FH en ambas copias
¿CÓMO SE
ASOCIA EL LDL CON LAS CÉLULAS DEL HÍGADO?
Para determinar si el LDL se enlaza con las células se
usaron etiquetas radioactivas. Los resultados de éste experimento fueron los
siguientes:
·
normales (+/+): las células enlazan cierta cantidad de
LDL
·
heterocigotos (FH/+): las células enlazan la MITAD del LDL de lo
normal
·
homocigotos (FH/FH): las células NO PUEDEN enlazarse con
LDL
Resultado:
- la mutación genética causa que el receptor LDL-R en la superficie de las células del hígado no funcione correctamente y no sea capaz de enlazar el LDL.
- por lo tanto, la cantidad de LDL libre en la sangre será mayor
- las personas homocigoto no tienen el receptor LDR-R en las células de su hígado, por lo tanto en éstas personas el hígado no es capaz de absorber el LDL de la sangre
- las personas heterocigoto producen una cantidad menor de receptores LDL-R en su sangre, y por lo tanto en éstas personas el hígado tiene una capacidad reducida de absorber el LDL de la sangre.
¿CÓMO SE DESCUBRIÓ
LA MUTACIÓN FH?
Para realmente entender la hipercolesteremia desde un
punto de vista de biología molecular, hay que identificar cuál es el gen que
está envuelto y la proteína (el receptor LDL-R) que es producido por éste gen.
Para lograr ésto :
· 1. un análisis bioquímico (assay) en el
que se expone el LDL a varios fragmentos de proteínas y entonces se purifican
las proteínas a las que el LDL se asocia
·
2. determinar la secuencia de
aminoácidos de esa proteína
·
3. una vez se tiene la secuencia de
aminoácidos, sintetizar oligonucleótidos (secuencias de ADN que corresponden a
la secuencia de aminoácidos) con etiquetas radioactivas
·
4. exponer esos oligonucleótidos
etiquetados a una biblioteca de ADN Complementario (ADNc), para encontrar
específicamente el gen que codifica el receptor LDL-R
·
5. expresar la proteína codificada por ese
gen usando la copia de la librería de ADNc, secuenciar la proteína, y
determinar que efectivamente tiene la misma secuencia de aminoácidos que la que
purificamos inicialmente.
·
6. una vez conocemos cuál es el gen,
tomar muestras de pacientes, aislar la copia del gen que éstos tienen, secuenciarla, y compararla con
la copia normal. Cuando se hizo esto se encontró que varias personas tenían mutaciones
en éste gen, y que al menos uno de los alelos mutantes, el FH, causa una
pérdida de función del receptor LDL-R.
·
7. de
esta manera también se descubrió la regulación del gen de HMG CoA
reductase
MEDICINA
RACIONAL - ESTRATEGIAS TERAPÉUTICAS
La medicina racional busca conocer los mecanismos
moleculares asociados con una condición de salud, entender los aspectos claves
como la genética y las rutas metabólicas bioquímicas (pathways) de éstos
mecanismos, identificar las proteínas y otras moléculas envueltas en éstos
mecanismos, y basado en éste conocimiento determinar si alguna de éstas
moléculas puede ser un blanco (target) que permita manipular el funcionamiento
del proceso bioquímico en la célula mediante una molécula con propiedades
terapéuticas : una medicina.
Una vez entendemos los mecanismos moleculares
asociados con la condición de hipercolesteremia, podemos idear estrategias:
1. Consumir menos colesterol
Ésto puede funcionar para personas (+/+) que consumen
un exceso de colesterol.
Resultado:
LDL en la sangre se reduce en aprox 10%.
No baja más porque una vez los niveles empiezan a bajar, el cuerpo produce más
colesterol.
2. Impedir que los ácidos bílicos se
reciclen, hacer que el cuerpo los excrete
Los ácidos bílicos están sintetizados a base de
colesterol. Una medicina que estimule la excreción de ácidos bílicos (en lugar
de reciclarlos) estimulará la producción de ácidos bílicos; esto hace que el
cuerpo use más colesterol y por lo tanto reduzca los niveles de colesterol
libre en la sangre. Se pueden usar medicinas basadas en resinas que se asocian
al ácido bílico para obligar al cuerpo a usar el colesterol para reponer éstos
ácidos bílicos.
Resultado:
LDL en la sangre se reduce en aprox 20%.
3. Bloquear la síntesis de colesterol
Para bloquear la síntesis de colesterol, tenemos que
estudiar la ruta metabólica ilustrada anteriormente, y determinar dónde es
posible bloquearla.
ácido acético (CH3 COOH) → acetil-CoA → (...etc...)
→ HMG-CoA → Mevolonate → (...etc...) →
colesterol ↑
HMG-CoA
reductase
Un posible target es el HMG-CoA reductase. Si logramos
bloquear o reducir la producción de ésta enzima, podemos reducir la producción de colesterol por parte de las células del
hígado. Además, una vez las células del hígado detectan que el nivel de LDL se
reduce, éstas aumentan la expresión del receptor LDL-R, lo cual aumenta la
captura de LDL libre en la sangre.
El resultado neto de (1) bloquear la síntesis de colesterol y (2) bloquear
el reuptake de colesterol, es una reducción de la cantidad de LDL libre
en la sangre.
Éstas medicinas existen, se llaman ESTATINAS. Las
estatinas son inhibidores de HMG-CoA
reductase.
Resultado: LDL
en la sangre se reduce en aprox 60%
En las personas +/+ y en las personas FH
heterocigotos, las estatinas logran una reducción de 60% en los niveles de LDL.
Sin embargo, las estatinas no funcionan
en las personas FH homocigotos, pues en éstas personas el gen que codifica el receptor
LDL-R no es funcional. Por lo tanto, aumentar la expresión de LDL-R no tiene
efecto en éstas personas.
PERO ESO ES
UNA HIPÓTESIS BASADA EN UNA CORRELACIÓN. ¿CÓMO DEMOSTRAMOS UNA RELACIÓN CAUSAL?
La relación causal entre los niveles de HDL y LDL con
las enfermedades cardiovasculares se han demostrado en pruebas clínicas
(clinical trials).
4S TRIAL
·
pacientes que tomaron medicinas que
reducen el LDL después de haber tenido un ataque al corazón exhibieron una
reducción en el riesgo de otro ataque. Ésto se conoce como “secondary prevention”.
WESTCOTT TRIAL
·
Se estudiaron pacientes con altos
niveles de LDL pero que no habían sufrido un ataque al corazón. Los que tomaron
estatinas exhibieron una reducción en la cantidad de ataques al corazón
comparados con los que no tomaron estatinas.
4. El gen PCSK9
Se ha descubierto que una forma mutante de éste gen
está asociado con una forma de hipercolesterolemia que se hereda de forma
mendeliana dominante. Las personas
que tienen el alelo mutante en una o ambas copias del gen tienen una alteración
en su función que causa hipercolesterolemia.
Si una forma mutada de éste gen causa
hipercolesterolemia, ¿qué ocurre si desactivamos (knock-out) el gen? Se estudiaron
personas con otro alelo mutante de éste gen, pero este alelo causaba pérdida de
función del gen. Éstas personas tenían un nivel de LDL en la sangre más bajo de
lo típico.
PCSK9 es una proteína soluble, y está envuelta en la
degradación del receptor LDL-R. Por lo tanto, una mutación en el gen que
produce PCSK9 que aumenta su expresión tendrá como efecto una menor cantidad de
receptores LDL-R en las células, y por lo tanto una mayor cantidad de LDL en la
sangre.
De la misma manera, una mutación que reduzca la expresión de PCSK9
reducirá la eliminación de los receptores; mientras más tiempo estén esos
receptores en la célula, más tiempo funcionarán sacando LDL de la sangre para
traerlo a la célula.
Esto convierte al PCSK9 es otro posible target para
una medicina para reducir el colesterol. Hay empresas trabajando en un anticuerpo
capaz de asociarse al PCSK9 y desactivarlo en personas sin las mutaciones. Varias
empresas están desarrollando éste tipo de drogas, entre ellas Amgen.
¿QUE TAL AUMENTAR
LOS NIVELES DE HDL?
¿Tendrá algún beneficio crear una medicina que aumente
los niveles de HDL? Tal vez, pero ésto es solamente una hipótesis. Hay que
obtener data experimental.
Pfizer desarrolló una droga que aumentaba el HDL, pero
no pudo demostrar en pruebas clínicas que ésto redujera las probabilidades de
un ataque al corazón.

